常见的口罩认证
新冠疫情在国内已经被控制住,控制疫情可以说很有一套。零星的局部病例可以在采取措施后很快得到控制。
但是,冬季来临前,国外已经迎来二次爆发,并且这次疫情的病例已经超过第一波的数量。如下图:
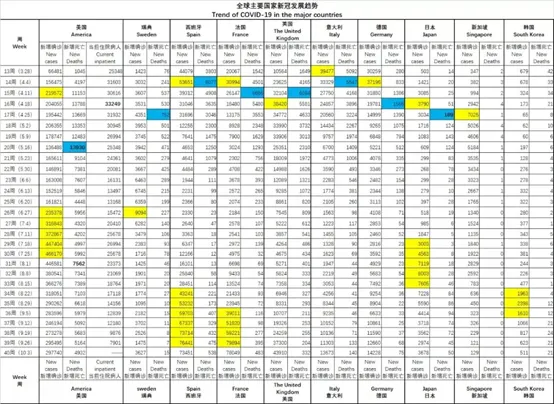
值得庆幸的是,死亡病例却比第一波大大降低,这个也符合疫情传播的规律,病毒朝着越来越弱的致病性进化。病毒越来越弱,无症状感染越来越多,死亡率下降。
作为重要的防疫物资,口罩是非常重要的。既然国内口罩需求打打减少,国外需要哪些认证呢?
1. 澳洲
民用防护口罩,可以申请AS/NZS 1716标准的个人防护产品认证。
AS/NZS 1716和欧标EN 149非常类似,和国标GB 2626也有很多类似的地方。澳标其实只需要测试盐性或者油性过滤效率的一种,不需要两个都测试。
AS/NZS 1716认证的流程主要步骤:
a. 填写申请表,明确需要申请的口罩规格和类型。
b.准备100个左右的样品寄送到实验室测试。
c. 测试的同时需要准备工厂审核,主要审核工厂的质量管理体系。
d. 工厂审核和测试都合格后,提交产品的资料就可以向澳洲机构申请发证书了。
此类证书一般5年有效,每年需要工厂审查,保证证书持续有效。
口罩TGA认证
澳大利亚药物管理局(Therapeutic Goods Administration),简称TGA。是澳洲卫生部所属的联邦bai药物主管机构
商品上市前的评估。所有药品、医疗器械在进入澳市场前,均要在TGA登记注册,对其风险进行评估
医用口罩属于低风险医疗器械,出口澳洲,必须申请TGA认证。
申请TGA认证,需要提供口罩的英文版测试报告,可以是澳标,欧标,国标,美标的。另外需要澳洲进口商,如果没有澳洲进口商,可以联系捡证网,我们可以提供。另外就是一些认证产品的资料,例如,材质清单,产品结构图,使用说明,等等。
欧盟CE认证
一般口罩分为两类,一类是个人防护类的PPE口罩,另一类是医用口罩。
首先说防护口罩,防护口罩类似于我们国内的KN95口罩,这类产品需要按照PPE Regulation (EU) 2016/425申请CE认证。
欧盟新法规PPE Regulation (EU) 2016/425已经实施,口罩属于“危及健康的物质和混合物”三类产品,必须按照MODULE B+MODULE C/D来申请认证,类似于旧法规的指令 89/686/EEC第10章 EC 型式检验第11章A/B节。
申请认证的步骤如下:
1. 确定申请产品的规格型号,耳带式,头带式,杯装,折叠等等规格。等级有FFP1,P2,P3等级。准备好产品说明书,选择有PPE发证资质的欧盟机构。欧盟有口罩认证资质的目前有30家左右,在国内做的比较多是bsi(0086,2797),SGS 0598,AENOR 0099,APPLUS 0370,CCQS 2834,APAVE 0082等等机构
 2. 准备测试样品。测试样品一般60个左右就可以,但是一般实验室要求准备100个样品。样品需要按照EN 149做全项目测试,包含泄漏率,油性和非油性过滤效率,呼吸阻力等等项目。具体测试要求根据等级不同而不同,可以咨询捡证网。
2. 准备测试样品。测试样品一般60个左右就可以,但是一般实验室要求准备100个样品。样品需要按照EN 149做全项目测试,包含泄漏率,油性和非油性过滤效率,呼吸阻力等等项目。具体测试要求根据等级不同而不同,可以咨询捡证网。
测试主要是申请MODULE B证书按照Type test来做。
3. 测试通过后,需要提交MODULE B的技术文件。主要包含,产品描述,口罩材质清单,结构图,口罩的质量控制计划,使用说明等等文件。如果不了解具体文件怎么准备,可以咨询捡证网。咨询电话:13636483412 QQ: 495226609
4.另外就是Module C2或者Module D的的后续监督认证。如果选择C2,需要在工厂抽样做测试。如果选择Module D,需要每年来工厂做审核,主要审核内容也是质量计划和质量管理体系。
5.以上步骤都通过后就可以拿到完整版的口罩CE证书了。在产品上加贴标签,出口欧盟。
以上就是防护类口罩申请CE认证的一些要求。
另外一种就是医用口罩申请CE认证,这种口罩大部分都是平面口罩,按照医疗器械法规来申请CE认证。主要流程如下:
1.确定医用口罩的名称和等级,产品等级可以分为TYPE I , II, IIR三个等级,下图是3个等级的测试要求。
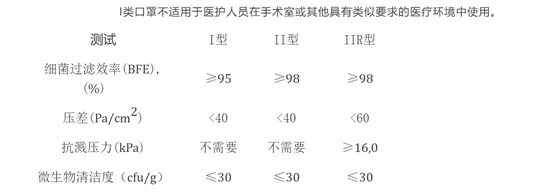 2. 医用口罩CE需要选择有资质的欧代,和欧代签订协议,一般是1-5年。欧代是口罩的欧盟代理方,如果产品有问题,欧盟官方首先会找欧代了解情况。
2. 医用口罩CE需要选择有资质的欧代,和欧代签订协议,一般是1-5年。欧代是口罩的欧盟代理方,如果产品有问题,欧盟官方首先会找欧代了解情况。
3. 准备医用口罩CE的样品测试,按照EN 14683:2019标准进行测试,准备大约80个样品。现在能够测试EN 14683的机构也比较多,有外资实验室,有CMA资质的实验室,也有CNAS资质的实验室。不同实验室价格和周期都不同。
4.测试合格以后,就可以把测试报告提交给欧代那边,让欧代去注册。注册的同时,还需要准备一套技术文件,包含产品的生物安排评估,产品使用说明,生物相容性等等。每个欧盟国家都可以去注册,我们常选择德国,西班牙,荷兰,法国等卫生部门去注册。不同国家注册的时间和费用不尽相同。
5.注册完成后就可以在医用口罩上打上CE认证标志。
同时国内还需要上商务局去申请白名单。白名单一般需要提供注册的文件给他们,另外就是DOC符合性声明,欧代协议,测试报告这些文件。
捡证网提供相关口罩CE认证咨询服务,咨询电话:13636483412 QQ: 495226609 邮箱:yangda@jz-cert.com